www.psychspace.com心理学空间网斯坦福神经调控疗法(Stanford Neuromodulation Therapy, SNT)
思影科技于 2022-03-24 10:59:20 发布
抑郁症是全世界致残的主要原因,一半的抑郁症患者患有难治性抑郁症。间歇性theta脉冲刺激 (Intermittent theta-burst stimulation, iTBS) 获美国食品和药物管理局批准,用于治疗难治性抑郁症,但其疗效不佳和持续时间为6周而受到限制。作者通过开发一种基于神经科学信息的加速iTBS方案——斯坦福神经调控疗法 (Stanford neuromodulation therapy, SNT;以前被称为斯坦福加速智能神经调控疗法Stanford accelerated intelligent neuromodulation therapy,简称SAINT),解决了这些局限性。该方案与开放标签治疗5天后约90%的缓解率相关。在这里,作者报告了SNT治疗难治性抑郁症的假刺激对照双盲试验结果。本文发表在American Journal of Psychiatry杂志。
方法:目前经历中度至重度抑郁发作的难治性抑郁症患者被随机分配接受真或假SNT治疗。静息态功能MRI用于个体化靶向左侧背外侧前额叶皮层与膝下前扣带皮层功能负相关最强的区域。主要结果为治疗4周后蒙哥马利-奥斯伯格抑郁评分量表(Montgomery-Åsberg Depression Rating Scale, MADRS)评分。
结果:在计划的中期 (interim) 分析中,32名难治性抑郁症患者被纳入,29名继续符合纳入标准的参与者接受了真(N=14)或假(N=15) SNT。治疗4周后,真治疗组MADRS评分较基线平均下降百分比为52.5%,假治疗组为11.1%。
结论:SNT是一种高剂量iTBS方案,以功能连接引导靶向治疗,比假刺激治疗难治性抑郁症更有效。还需要进一步的试验来确定SNT的耐用性,并将其与其他治疗方法进行比较。
1.引言
重度抑郁症是全球致残的主要原因,约50%的患者符合难治性抑郁症的标准。重复经颅磁刺激 (Repetitive transcranial magnetic stimulation, rTMS),一种经美国食品和药物管理局(Food and Drug Administration, FDA) 批准的治疗难治性抑郁症的脑刺激疗法,靶向于左背外侧前额叶皮层 (dorsolateral prefrontal cortex, DLPFC),该区域是抑郁症神经回路的一个关键区域,已被证明在重度抑郁症中是低活性的 (hypoactive)。当代FDA批准的刺激左侧DLPFC的方案受到长疗程 (6周) 的限制,并且只有中等效果,约17%的患者 (这些患者对之前的三种抗抑郁药物治疗没有反应) 在治疗4-6周后产生缓解。
我们开发了一种加速、高剂量、模式化、功能连接MRI (functional connectivity MRI, fcMRI) 引导的rTMS方案,旨在利用神经科学信息指导刺激参数,优化难治性抑郁症的治疗。我们的方案以前被称为斯坦福加速智能神经调控疗法(Stanford accelerated intelligent neuromodulation therapy, SAINT),现在被称为斯坦福神经调控疗法 (Stanford neuromodulation therapy, SNT),包括:
1) 一种有效的rTMS形式,称为间歇性theta脉冲刺激 (intermittent theta-burst stimulation, iTBS);
2) 每天以最佳间隔进行多次iTBS治疗;
3) 应用更高的总脉冲刺激剂量;
4) 个性化靶向刺激左侧DLPFC至膝下前扣带皮层 (subgenual anterior cingulate cortex, sgACC)回路。
我们的SNT方案的开放标签试验显示,即使在难治性抑郁症患者中缓解率也达到了约90%,该缓解率几乎是目前难治性抑郁症金标准疗法 (ECT) 缓解率 (48%) 的两倍。然而,SNT的疗效尚未在随机假对照试验中进行研究。在本研究中,我们研究了SNT的抗抑郁疗效,并将其与相同的假刺激方案进行比较,以确定安慰剂效应的作用。
2. 方法
2.1 研究设计
我们采用平行设计进行了1:1双盲随机对照研究。该试验已在美国临床试验注册中心(NCT03068715) 进行了前瞻性注册。所有程序都是按照《赫尔辛基宣言》所概述的道德标准进行的。这项研究得到了斯坦福大学机构审查委员会的批准。所有参与者在参与任何研究程序之前都提供了书面同意。
在效力 (power) 分析的基础上,我们计划招募60名参与者参与这项试验。我们计划在30名参与者接受治疗后进行中期分析。
【Power分析】样本量越大,越容易找到差异。但实验有成本,因此需要Power值指导实验设计人员判断出实验需要多少样本。使用该样本量,有一定概率找到差异,且可以不浪费人力物力。可以通过工具包实现power分析,如Python的statsmodels.stats.power。
2.2 参与者
该研究于2017年3月至2019年12月在斯坦福大学精神病学部门进行。我们招募了初步诊断为重度抑郁症的个体,他们目前处于中度到重度抑郁(17-项汉密尔顿抑郁量表[17-item Hamilton Depression Rating Scale, HAM-D]和蒙哥马利-奥斯伯格抑郁量表[Montgomery-Åsberg Depression Rating Scale, MADRS]得分≥20),22至80岁,根据Maudsley分期法测定,具有中度至重度难治性水平。在治疗前4周,参与者被要求保持稳定的抗抑郁药物治疗方案,或保持无药物治疗,并在整个研究过程中保持该方案 (包括5天治疗方案后的所有随访评估)。如果潜在参与者有除重度抑郁症以外的任何主要精神病诊断或接受iTBS后可能存在风险的情况,则将其排除在外。此外,还排除了曾接触过rTMS、对ECT无反应或有抑郁症精神外科史的参与者。
2.3 成像
在接受SNT之前,每个参与者都采集了结构MRI和静息态fMRI。
【补充材料】
利用基于组织概率的统计参数(Statistical Parametric Mapping, SPM)分割方法,计算估计参数,将T1加权结构图像输入到MNI。然后将配准矩阵翻转,用于将标准空间的左侧D LPFC (Brodmann area 46)和sgACC (Brodmann area 25)配准到个体被试的大脑中。然后将配准到参与者空间的ROIs做重采样、平滑和二值化,以匹配静息态扫描的维度。
所有的分析都是在参与者自己的大脑空间中进行的。所有预处理均采用SPM12软件。使用两个独立的算法确定被试空间左侧DLPFC ROI的个体化靶点位置:
第一种算法使用层次聚类算法,通过计算左侧DLPFC和sgACC ROI内的所有体素提取的体素之间的时间序列相关来进行聚类,寻找到那些和所有体素中中位数时间序列最相似的体素,将它们在个体上保留下来作为个体的功能区。
第二种算法基于三个因素确定最优的左侧DLPFC靶点:左侧DLPFC和sgACC的网络相关/负相关(体素水平)、亚单元的大小、亚单元的空间集中度。
2.4 临床评估
在筛选时、基线检查时、SNT结束后的下一个工作日 (治疗后立即) 以及SNT结束后的1、2、3和4周进行评估。主要结果为治疗后4周(第5周)的MADRS评分,归一化至基线(第0周)。如果参与者的MADRS评分从筛查到基线评估的变化大于或等于30%,则被排除。
次要临床结果量表包括16-项抑郁症状自我报告快速量表 (Quick Inventory of Depressive Symptomatology–Self-Report, QIDS-SR) 和6-项、17-项汉密尔顿抑郁量表(Hamilton Depression Rating Scales, HAM-D)。在所有主要时间点分别使用青年躁狂量表 (Young Mania Rating Scale, YMRS) 和自杀意念量表来评估与躁狂和自杀相关的安全性。在基线和治疗后立即进行一系列测试,评估潜在的神经认知副作用,其中包括霍普金斯语言学习测试和Delis-Kaplan执行功能系统的子测试:追踪测试和颜色词干扰测试(详细信息请参阅补充材料)。
2.5 SNT方案
参与者被随机分配接受真或假SNT。所有治疗均使用MagVenture MagPro X100系统,该系统配备双面MagVenture Cool-B65 A/P线圈。在每个疗程中,使用Localite神经导航系统将TMS线圈定位在个性化刺激靶点上。连续5天,每天治疗10次,总计18000次脉冲/天(详情见我们之前关于开放标签治疗的报告)。以静息运动阈值(resting motor threshold, rMT)的90%进行刺激,并根据识别的fcMRI靶点深度进行调整。为每个个体创建的个性化靶点位于不同的皮层深度。由于感应电场的强度随着距TMS线圈距离的增加而减小,因此使用了深度校正强度,目的是将相当于90% rMT的强度传递给所有个性化靶点。为了安全起见,刺激强度从未超过rMT的120%。
2.6 盲法
所有参与者、临床评估者、治疗提供者和其他研究人员都是不知道治疗任务的。临床评估者和治疗提供者是不同的人。参与者被要求不要与研究人员讨论刺激感受。所有iTBS治疗使用相同的刺激线圈,没有真或假定向的迹象。一次性水凝胶胶垫电极(“假垫”)被用来传递同步直流电刺激来模拟真刺激的感觉。前七名参与者的假刺激垫直接放置在治疗线圈的下方;然而,由于与脑电图设备不兼容,这一做法被终止。剩下的22名参与者戴着降噪耳机(Sennheiser CX300S,带记忆泡沫头),连接到假噪音发生器(MagVenture A/S),以模拟每个参与者在可容忍的最大噪音强度下的刺激噪声模式。此外,利多卡因(lidocaine)应用于刺激部位以减少感觉。为了保持TMS操作者不知道真假治疗,在每次iTBS治疗开始前,在线圈的一侧固定一个覆盖物,并将其放置在适当位置,以限制真刺激导致的任何潜在面部肌肉或下颌运动。在每个刺激过程中,所有参与者都能看到显示器,显示他们的fcMRI引导的靶点。如果多名研究参与者同时在门诊,他们被安排在不同的等候区,并被告知不要互相交谈。
2.7 盲法完整性分析
参与者被要求猜测他们的治疗分配,并在治疗的最后一天报告他们对自己的猜测的信心(在1到5的范围内)。创建了一个猜测指标,范围从0 (参与者接受假刺激的充分信心) 到1 (参与者接受真刺激的充分信心)。随机猜测的平均分是0.5分。用单向t检验评估偏离随机猜测的情况。因为不是所有的参与者都表明了他们的信心,所以二项测试也被用来确定正确猜测的次数是否超过了随机水平。最后,使用线性回归分析来评估猜测指标和抑郁症严重程度变化 (MADRS评分与基线相比的百分比变化) 之间的关系。
2.8 用于靶点生成的fMRI分析
每个参与者的个性化左侧DLPFC靶点使用基线静息态扫描生成,方法与之前报道的相同。靶点位置见图1。
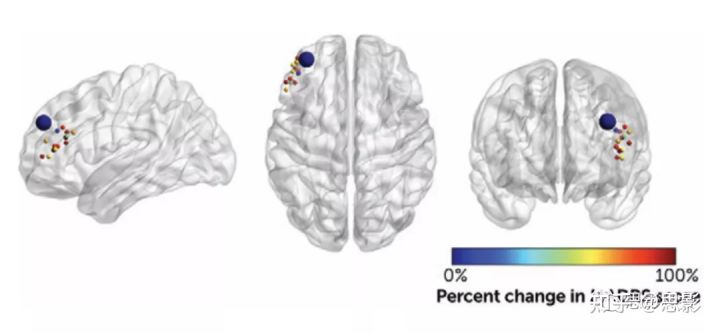
图1个体化功能连接MRI引导的靶点定位用于斯坦福神经调控治疗的靶点位置与平均F3坐标的关系
2.9临床结果分析
所有统计分析均使用SPSS 27版进行。我们的主要结果测量是治疗后4周的MADRS评分,归一化至基线。用MADRS评分计算各组的响应率(response)和缓解率(remission)。响应定义为MADRS评分下降至少50%,缓解定义为MADRS评分下降不大于10。在4周的随访中,如果参与者在任何时候满足了这些特定的症状,他们就被认定为响应者或缓解者。选择这种方法,而不是选择在单一时间点的响应或缓解,可以考虑不同的响应轨迹。这种计算响应率和缓解率的方法是专门选择的,作为重度抑郁症快速治疗疗法开发的一部分,这种快速治疗与全面的长期治疗相结合,以保持参与者处于缓解状态。因此,该方法的缓解率最相关的衡量指标是在治疗后一个月内任何时间点进入缓解期的个体比例,无论他们是在治疗后立即进入缓解期还是在延迟反应轨迹后进入缓解期,因为不管治疗轨迹如何,都会进行维持治疗。6-项HAM-D、17-项HAM-D和QIDS-SR得分的变化被用作抑郁严重程度的次要测量指标。初始线性混合模型产生的残差不是正态分布的(通过Shapiro-Wilk检验评估)。因此,使用广义线性混合模型评估MADRS、6-项HAM-D、17-项HAM-D和QIDS-SR得分的变化,该模型使用Satterthwaite自由度近似和稳健系数估计来处理违反模型假设的情况。评估时间、治疗组(真或假)的固定效应和交互效应。除模型不收敛或收敛于非实解的情况外,所有分析均采用复合对称协方差结构。在这些情况下,使用了自回归协方差结构。所有事后两两比较都经过了Bonferroni校正。类似的广义线性混合模型被用于分析潜在的神经认知副作用。
3结果
3.1被试特征
试验在中点停止,因为计划的中期分析表明,与假刺激相比,真刺激的效应值较大(Cohen’d>0.8)。因此,这里报告的结果来自于进入试验直至中期分析的参与者样本。
共有182人通过在线筛查数据库进行了资格评估,其中54人接受了现场筛查。32名参与者进行了随机分组;然而,其中两名参与者没有被纳入,一名因为不再符合纳入标准而退出,另一名因为厌恶可能被分配到假刺激组而退出。剩下的30名参与者以1:1的比例被分配接受真或假SNT。在纳入后,另一名参与者被发现不符合纳入标准。因此,符合纳入标准、加入试验并同意接受真或假治疗的两组参与者的最终人数分别为真SNT组14人和假SNT组15人(图2)。两组的人口统计学特征相似(表1)。两组的既往抗抑郁药物试验数量(均值=5,SD=2)和Maudsley分期法总得分(均值=9,SD=2;中度抗药性)相同。所有参与者都完成了全面治疗和治疗后即刻评估。两组各有1例患者未完成4周随访。假治疗组的一名参与者在研究入组后,SNT治疗周前2周开始服用一种新的药物(5 -羟色胺-肾上腺素再摄取抑制剂),在整个试验中一直保持亚治疗剂量水平。所有的分析都包括了这个参与者。
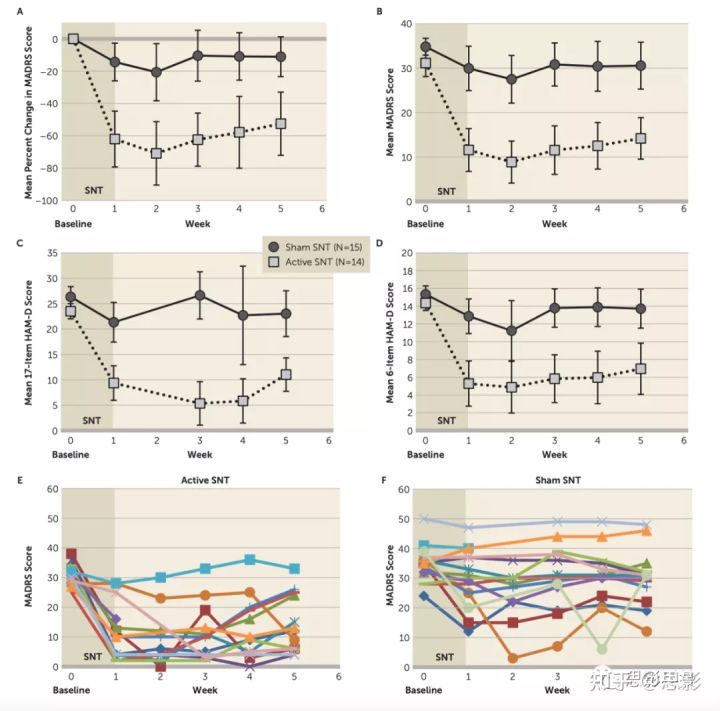
图2难治性抑郁症患者真或假斯坦福神经调控治疗(Stanford neuromodulation therapy, SNT)前后的抑郁评分
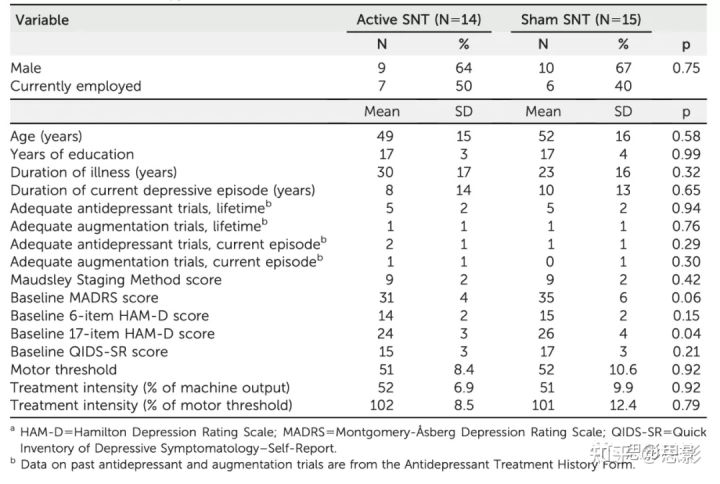 表1 斯坦福神经调控治疗(Stanford neuromodulation therapy, SNT)双盲随机对照试验参与者的特征
表1 斯坦福神经调控治疗(Stanford neuromodulation therapy, SNT)双盲随机对照试验参与者的特征
3.2效力(Efficacy)
最初的主要结果是5天SNT治疗结束后4周的MADRS评分。评分归一化到治疗前基线,即以基线值的百分比表示。真刺激组治疗后0周、1周、2周、3周和4周的意向治疗(intention-to-treat) MADRS得分的平均降低百分比是基线的62.0%、70.9%、62.4%、57.8%、52.5%,假刺激组是14.3%、20.6%、10.4%、10.9%和11.1%,效应值(Cohen’s d)分别为1.7、1.4、1.8、1.5、1.4。由于参与者的响应轨迹不同,响应率和缓解率随随访时间点而变化。总的来说,在4周的随访中,真SNT组中有12名(85.7%)参与者符合响应标准(MADRS评分降低超过50%),11名(78.6%)参与者在5个治疗后评估中至少有一个达到缓解标准(MADRS评分不大于10)。在假治疗组,4周随访期间,4名参与者(26.7%)有反应,2名参与者(13.3%)在某个时间点缓解。真治疗组治疗后0、1、2、3、4周的缓解率和响应率分别为57.1%和71.4%;66.7%和77.8%;53.8%和84.6%;61.5%和69.2%;46.2%和69.2%。假刺激的缓解率和响应率分别为0%和13.3%;10.0%和20.0%;7.1%和7.1%;7.1%和7.1%;0%和7.1%。
广义线性混合模型显示,在MADRS评分上,治疗组(F=24.8, df=1, 14, p<0.001)、时间(F=16.1, df=5, 24, p<0.001)的主效应显著,治疗组与时间(F=6.1, df=5, 24, p<0.001)的交互效应显著。真治疗组的参与者在所有随访时间点的MADRS评分在治疗后显著降低(Bonferroni校正p<0.05)。对于次要结果(6-项HAM-D、17-项HAM-D和QIDS-SR得分的变化)、使用上次观察结转法(last-observation-carried-forward method)估算的缺失数据模型,以及使用原始评分而不是基线评分时,发现了等价的结果。
3.3盲法的完整性
23名参与者猜测了他们所接受的是哪种治疗,19名参与者表示对自己的猜测有信心。单因素t检验表明,假刺激组(平均猜值=0.39,p=0.56)和真刺激组(平均猜值=0.43,p=0.52)的随机性(随机值=0.50)没有显著差异。因为并不是所有的参与者都对自己的猜测有信心,所以二项测试也被用来确定正确猜测的次数是否超过了随机水平。二项测试表明,在假刺激(6/10正确,p=0.38)和真刺激组(7/13正确,p=0.50)中,正确猜测的比例与随机水平没有显著差异。在MADRS评分中,猜测度量和评分比例变化幅度之间没有关系(r=0.11, p=0.66)。因为使用了两种假刺激方法,我们还测试了两种方法之间的差异,即正确猜测自己属于假治疗组的参与者的比例,我们发现没有显著差异(Fisher的确切测试,p=0.12)。此外,在广义线性混合模型中纳入假刺激类型并没有改变结果,假刺激类型或假刺激类型与时间的相互作用也不是一个显著因素(假刺激类型:F=0.2, df=1,21, p=0.68;治疗组:F=26.6, df=1, 19, p<0.001;时间:F=13.2, df=5, 38, p<0.001;治疗组-时间交互作用:F=5.8, df=5, 33, p=0.001;假刺激类型与时间的交互作用:F=1.9, df=4, 29, p=0.14)。
3.4安全性
试验期间未发生严重不良事件。每天记录自发的副作用,并按常见的rTMS副作用进行分类。如果不适只发生在刺激过程中,而在SNT后没有持续,则记录“治疗部位不适”;如果不适在治疗后持续,则记录“SNT后头痛”。与假刺激组相比,真刺激组的唯一副作用发生率接近统计学意义的是头痛(Fisher确切检验,p<0.06)。所有头痛自行缓解或在服用非处方止痛药(如布洛芬)后缓解。两组患者最常见的副作用是疲劳。在另一项试验中,一名参与者经历了牙齿脱落,之后我们改变了实验室中所有试验的牙齿安全协议,包括目前的试验。
从基线到治疗后即刻评估,真假治疗组均表现出稳定的认知测试表现。语言加工速度(颜色单词阅读完成时间)存在组别和时间的显著交互作用(F=4.7, 1,21, p=0.04),随后的Bonferroni校正的事后比较显示,真刺激组有显著改善(F=5.5, df=1,21, p=0.03),假刺激组没有(F=0.4, df=1,21, p=0.54)。所有其他测量显示,组别和时间的交互作用不显著。
4.讨论
本研究的目的是研究SNT的抗抑郁疗效,SNT是一种加速、高剂量、模式化、fcMRI指导的iTBS方案,用于治疗难治性抑郁症。参与者对治疗的耐受性良好;所有参与者都完成了5天的疗程,副作用与常规每日rTMS相似,真SNT组的头痛发生率高于假治疗组。头痛是TMS治疗方案中最常见的副作用之一,所以这是预期的副作用;我们的真治疗组的头痛发生率(57%)与FDA批准的治疗难治性抑郁症的标准iTBS方案(65%)相似。
我们观察到SNT有很大的抗抑郁作用。经过5天的治疗后,真SNT组79%的参与者(14名参与者中的11名)在4周的随访中在某个时间点抑郁发作得到缓解,而假治疗组只有13% (15名参与者中的2名)。SNT治疗疗程短,抗抑郁疗效高,为需要快速治疗的急诊或住院患者提供了治疗机会。
SNT的大效应可能是由几个因素造成的。SNT方案是根据神经科学信息的刺激参数设计的,并被选择以最佳方式调节目标神经回路。
首先,fcMRI引导的靶向策略用于刺激每个个体中与sgACC最负相关的左侧DLPFC区域。
第二,刺激每小时进行一次,因为50到90分钟的间隔已经被证明对突触强化产生累积效应。相比之下,间隔40分钟或更短的间隔不会产生累积效应。
第三,我们以静息运动阈值(rMT)的90%的强度进行刺激,并根据靶区皮层深度的个体差异进行调整,而不是FDA批准的rMT强度的120%,因为90%的rMT强度下,传递1800次脉冲可能更有效地诱导皮质兴奋性的改变由此产生的功能连通性改变。
第四,每个iTBS治疗发出1800次脉冲,而不是典型的600次脉冲,因为在90%的rMT强度下,1800次iTBS脉冲已被证明在皮质兴奋性方面产生更大的变化。此外,一项使用1800次脉冲的盲法iTBS试验仅在2周内就产生了有效的抗抑郁反应,这比FDA批准的使用600次脉冲的标准iTBS方案要快。最后,SNT方案被设计为提供比标准iTBS方案更高的总脉冲剂量(90000和18000次脉冲),因为更高的脉冲剂量与更大的抗抑郁疗效相关。SNT参数的选择在我们之前的出版物中进行了详细的讨论。
尽管我们的受试者样本中抑郁症状的严重程度和难治性水平很高,并且在1个月的随访中进行了计算,但仍观察到SNT的抗抑郁作用量很大。更严重的抑郁症状和更高水平的难治性都与rTMS反应较差有关。我们研究的参与者平均有五次适当的抗抑郁药物试验;传统的rTMS疗法被发现只有17%的患者有缓解,这些患者之前对三种抗抑郁药物治疗没有反应。此外,62%的参与者有复发性抑郁发作,而不是连续发作,这也被证明对rTMS治疗后的结果有负面预测。与rTMS研究中假治疗通常报告的缓解率相比,在我们的样本中,高水平的治疗耐药性也可能是我们假治疗组的缓解率相对较低的原因(13%);之前的一项假对照iTBS研究表明,中度至重度治疗抵抗的个体对假治疗的反应最小。
在这份报告中,我们包括了整个4周随访期的响应率和缓解率。这与其他iTBS抑郁症临床试验中更常见的单时间点响应或缓解标准不同。我们认为,基于SNT作为抑郁症状潜在神经回路的探针和预期的未来临床方法,这种定义二分类结果的方法是合适的。这些高的总体响应率和缓解率提供了进一步的证据,支持左侧DLPFC-sgACC网络的功能障碍是抑郁症状的主要神经基础。本研究在文献的基础上进行了扩展,证明当使用优化的刺激剂量和模式来定位该回路时,绝大多数个体(本研究中85.7%)将在一段时间内产生抗抑郁反应。由于未知的原因,参与者在SNT过程中显示出不同的反应轨迹(见图2E),这在rTMS和iTBS中已被报道。作为一种治疗工具,SNT仍在开发中。我们提出了一种治疗模式,在这种治疗模式中,SNT被用于快速缓解抑郁症,随后进行强度较小的维持治疗,可以采用任何有效和可接受的方式——药物、心理治疗、脑刺激和其他治疗。在这种治疗模式下,所有在治疗后一个月进入缓解期的患者都可以过渡到维持治疗。因此,通过在4周随访期间任何一周内符合这些标准的所有参与者来计算响应率和缓解率是合适的。
这项研究有一些局限性:
首先,由于真治疗组的优势和较大的效应量,试验在计划的中期分析时结束,因此,样本量小;然而,样本量与其他针对严重难治性抑郁症患者的临床试验的样本量相似。
其次,与所有重度抑郁症的临床试验一样,我们的研究依赖于临床评估来衡量抑郁症症状的改善,因为目前还没有抑郁症缓解的有效生物标志物。
第三,到目前为止,我们的SNT方案已经在一个单一的地点,在一个受过高等教育的样本中进行了测试。虽然这限制了推广,但在这个治疗抵抗人群中没有显著的假反应,表明真刺激对这个患者群体的疗效明显优于假刺激。
第四,45%的参与者样本有精神疾病共病,这可能会影响方案的有效性。尤其是共病焦虑会降低rTMS的效力,也许是因为这些患者需要一个替代的治疗靶点或该人群中苯二氮卓类药物使用率更高。然而,真治疗组和假治疗组共病精神疾病的参与者人数没有显著差异。
最后,考虑到与其他TMS方案相比,在类似人群中效果较大,我们假设SNT和标准rTMS方案之间的差异导致了较高的抗抑郁疗效;然而,SNT仍需直接针对另一种真刺激方案进行测试,SNT方案在改善传统iTBS疗效方面的独特性仍有待确定。需要进行研究,比较有无fcMRI引导靶向的SNT参数的有效性,以确定这种靶向方法的重要性。
总之,在难治性样本中,经过5天的治疗后,与相同的假刺激疗程相比,SNT能显著降低抑郁症状。短时间和高抗抑郁效果的SNT可以在紧急或住院情况下治疗患者,在这种情况下压缩时间过程是必要的。
总结:
本文提出了个性化斯坦福神经调控疗法,作者使用静息态功能MRI定位个体化靶点,即左侧背外侧前额叶皮层与膝下前扣带皮层功能负相关最强的区域。该个体化靶点用于难治性抑郁症患者治疗,比假刺激治疗更有效。该疗法加速、高剂量、模式化、以功能连接为指导确定个体化靶点,疗程短,抗抑郁疗效高,为需要快速治疗的急诊或住院患者提供了治疗机会
————————————————
版权声明:本文为CSDN博主「思影科技」的原创文章,遵循CC 4.0 BY-SA版权协议,转载请附上原文出处链接及本声明。
原文链接:https://blog.csdn.net/cc1609130201/article/details/123705647www.psychspace.com心理学空间网
思影科技于 2022-03-24 10:59:20 发布
抑郁症是全世界致残的主要原因,一半的抑郁症患者患有难治性抑郁症。间歇性theta脉冲刺激 (Intermittent theta-burst stimulation, iTBS) 获美国食品和药物管理局批准,用于治疗难治性抑郁症,但其疗效不佳和持续时间为6周而受到限制。作者通过开发一种基于神经科学信息的加速iTBS方案——斯坦福神经调控疗法 (Stanford neuromodulation therapy, SNT;以前被称为斯坦福加速智能神经调控疗法Stanford accelerated intelligent neuromodulation therapy,简称SAINT),解决了这些局限性。该方案与开放标签治疗5天后约90%的缓解率相关。在这里,作者报告了SNT治疗难治性抑郁症的假刺激对照双盲试验结果。本文发表在American Journal of Psychiatry杂志。
方法:目前经历中度至重度抑郁发作的难治性抑郁症患者被随机分配接受真或假SNT治疗。静息态功能MRI用于个体化靶向左侧背外侧前额叶皮层与膝下前扣带皮层功能负相关最强的区域。主要结果为治疗4周后蒙哥马利-奥斯伯格抑郁评分量表(Montgomery-Åsberg Depression Rating Scale, MADRS)评分。
结果:在计划的中期 (interim) 分析中,32名难治性抑郁症患者被纳入,29名继续符合纳入标准的参与者接受了真(N=14)或假(N=15) SNT。治疗4周后,真治疗组MADRS评分较基线平均下降百分比为52.5%,假治疗组为11.1%。
结论:SNT是一种高剂量iTBS方案,以功能连接引导靶向治疗,比假刺激治疗难治性抑郁症更有效。还需要进一步的试验来确定SNT的耐用性,并将其与其他治疗方法进行比较。
1.引言
重度抑郁症是全球致残的主要原因,约50%的患者符合难治性抑郁症的标准。重复经颅磁刺激 (Repetitive transcranial magnetic stimulation, rTMS),一种经美国食品和药物管理局(Food and Drug Administration, FDA) 批准的治疗难治性抑郁症的脑刺激疗法,靶向于左背外侧前额叶皮层 (dorsolateral prefrontal cortex, DLPFC),该区域是抑郁症神经回路的一个关键区域,已被证明在重度抑郁症中是低活性的 (hypoactive)。当代FDA批准的刺激左侧DLPFC的方案受到长疗程 (6周) 的限制,并且只有中等效果,约17%的患者 (这些患者对之前的三种抗抑郁药物治疗没有反应) 在治疗4-6周后产生缓解。
我们开发了一种加速、高剂量、模式化、功能连接MRI (functional connectivity MRI, fcMRI) 引导的rTMS方案,旨在利用神经科学信息指导刺激参数,优化难治性抑郁症的治疗。我们的方案以前被称为斯坦福加速智能神经调控疗法(Stanford accelerated intelligent neuromodulation therapy, SAINT),现在被称为斯坦福神经调控疗法 (Stanford neuromodulation therapy, SNT),包括:
1) 一种有效的rTMS形式,称为间歇性theta脉冲刺激 (intermittent theta-burst stimulation, iTBS);
2) 每天以最佳间隔进行多次iTBS治疗;
3) 应用更高的总脉冲刺激剂量;
4) 个性化靶向刺激左侧DLPFC至膝下前扣带皮层 (subgenual anterior cingulate cortex, sgACC)回路。
我们的SNT方案的开放标签试验显示,即使在难治性抑郁症患者中缓解率也达到了约90%,该缓解率几乎是目前难治性抑郁症金标准疗法 (ECT) 缓解率 (48%) 的两倍。然而,SNT的疗效尚未在随机假对照试验中进行研究。在本研究中,我们研究了SNT的抗抑郁疗效,并将其与相同的假刺激方案进行比较,以确定安慰剂效应的作用。
2. 方法
2.1 研究设计
我们采用平行设计进行了1:1双盲随机对照研究。该试验已在美国临床试验注册中心(NCT03068715) 进行了前瞻性注册。所有程序都是按照《赫尔辛基宣言》所概述的道德标准进行的。这项研究得到了斯坦福大学机构审查委员会的批准。所有参与者在参与任何研究程序之前都提供了书面同意。
在效力 (power) 分析的基础上,我们计划招募60名参与者参与这项试验。我们计划在30名参与者接受治疗后进行中期分析。
【Power分析】样本量越大,越容易找到差异。但实验有成本,因此需要Power值指导实验设计人员判断出实验需要多少样本。使用该样本量,有一定概率找到差异,且可以不浪费人力物力。可以通过工具包实现power分析,如Python的statsmodels.stats.power。
2.2 参与者
该研究于2017年3月至2019年12月在斯坦福大学精神病学部门进行。我们招募了初步诊断为重度抑郁症的个体,他们目前处于中度到重度抑郁(17-项汉密尔顿抑郁量表[17-item Hamilton Depression Rating Scale, HAM-D]和蒙哥马利-奥斯伯格抑郁量表[Montgomery-Åsberg Depression Rating Scale, MADRS]得分≥20),22至80岁,根据Maudsley分期法测定,具有中度至重度难治性水平。在治疗前4周,参与者被要求保持稳定的抗抑郁药物治疗方案,或保持无药物治疗,并在整个研究过程中保持该方案 (包括5天治疗方案后的所有随访评估)。如果潜在参与者有除重度抑郁症以外的任何主要精神病诊断或接受iTBS后可能存在风险的情况,则将其排除在外。此外,还排除了曾接触过rTMS、对ECT无反应或有抑郁症精神外科史的参与者。
2.3 成像
在接受SNT之前,每个参与者都采集了结构MRI和静息态fMRI。
【补充材料】
利用基于组织概率的统计参数(Statistical Parametric Mapping, SPM)分割方法,计算估计参数,将T1加权结构图像输入到MNI。然后将配准矩阵翻转,用于将标准空间的左侧D LPFC (Brodmann area 46)和sgACC (Brodmann area 25)配准到个体被试的大脑中。然后将配准到参与者空间的ROIs做重采样、平滑和二值化,以匹配静息态扫描的维度。
所有的分析都是在参与者自己的大脑空间中进行的。所有预处理均采用SPM12软件。使用两个独立的算法确定被试空间左侧DLPFC ROI的个体化靶点位置:
第一种算法使用层次聚类算法,通过计算左侧DLPFC和sgACC ROI内的所有体素提取的体素之间的时间序列相关来进行聚类,寻找到那些和所有体素中中位数时间序列最相似的体素,将它们在个体上保留下来作为个体的功能区。
第二种算法基于三个因素确定最优的左侧DLPFC靶点:左侧DLPFC和sgACC的网络相关/负相关(体素水平)、亚单元的大小、亚单元的空间集中度。
2.4 临床评估
在筛选时、基线检查时、SNT结束后的下一个工作日 (治疗后立即) 以及SNT结束后的1、2、3和4周进行评估。主要结果为治疗后4周(第5周)的MADRS评分,归一化至基线(第0周)。如果参与者的MADRS评分从筛查到基线评估的变化大于或等于30%,则被排除。
次要临床结果量表包括16-项抑郁症状自我报告快速量表 (Quick Inventory of Depressive Symptomatology–Self-Report, QIDS-SR) 和6-项、17-项汉密尔顿抑郁量表(Hamilton Depression Rating Scales, HAM-D)。在所有主要时间点分别使用青年躁狂量表 (Young Mania Rating Scale, YMRS) 和自杀意念量表来评估与躁狂和自杀相关的安全性。在基线和治疗后立即进行一系列测试,评估潜在的神经认知副作用,其中包括霍普金斯语言学习测试和Delis-Kaplan执行功能系统的子测试:追踪测试和颜色词干扰测试(详细信息请参阅补充材料)。
2.5 SNT方案
参与者被随机分配接受真或假SNT。所有治疗均使用MagVenture MagPro X100系统,该系统配备双面MagVenture Cool-B65 A/P线圈。在每个疗程中,使用Localite神经导航系统将TMS线圈定位在个性化刺激靶点上。连续5天,每天治疗10次,总计18000次脉冲/天(详情见我们之前关于开放标签治疗的报告)。以静息运动阈值(resting motor threshold, rMT)的90%进行刺激,并根据识别的fcMRI靶点深度进行调整。为每个个体创建的个性化靶点位于不同的皮层深度。由于感应电场的强度随着距TMS线圈距离的增加而减小,因此使用了深度校正强度,目的是将相当于90% rMT的强度传递给所有个性化靶点。为了安全起见,刺激强度从未超过rMT的120%。
2.6 盲法
所有参与者、临床评估者、治疗提供者和其他研究人员都是不知道治疗任务的。临床评估者和治疗提供者是不同的人。参与者被要求不要与研究人员讨论刺激感受。所有iTBS治疗使用相同的刺激线圈,没有真或假定向的迹象。一次性水凝胶胶垫电极(“假垫”)被用来传递同步直流电刺激来模拟真刺激的感觉。前七名参与者的假刺激垫直接放置在治疗线圈的下方;然而,由于与脑电图设备不兼容,这一做法被终止。剩下的22名参与者戴着降噪耳机(Sennheiser CX300S,带记忆泡沫头),连接到假噪音发生器(MagVenture A/S),以模拟每个参与者在可容忍的最大噪音强度下的刺激噪声模式。此外,利多卡因(lidocaine)应用于刺激部位以减少感觉。为了保持TMS操作者不知道真假治疗,在每次iTBS治疗开始前,在线圈的一侧固定一个覆盖物,并将其放置在适当位置,以限制真刺激导致的任何潜在面部肌肉或下颌运动。在每个刺激过程中,所有参与者都能看到显示器,显示他们的fcMRI引导的靶点。如果多名研究参与者同时在门诊,他们被安排在不同的等候区,并被告知不要互相交谈。
2.7 盲法完整性分析
参与者被要求猜测他们的治疗分配,并在治疗的最后一天报告他们对自己的猜测的信心(在1到5的范围内)。创建了一个猜测指标,范围从0 (参与者接受假刺激的充分信心) 到1 (参与者接受真刺激的充分信心)。随机猜测的平均分是0.5分。用单向t检验评估偏离随机猜测的情况。因为不是所有的参与者都表明了他们的信心,所以二项测试也被用来确定正确猜测的次数是否超过了随机水平。最后,使用线性回归分析来评估猜测指标和抑郁症严重程度变化 (MADRS评分与基线相比的百分比变化) 之间的关系。
2.8 用于靶点生成的fMRI分析
每个参与者的个性化左侧DLPFC靶点使用基线静息态扫描生成,方法与之前报道的相同。靶点位置见图1。

图1个体化功能连接MRI引导的靶点定位用于斯坦福神经调控治疗的靶点位置与平均F3坐标的关系
2.9临床结果分析
所有统计分析均使用SPSS 27版进行。我们的主要结果测量是治疗后4周的MADRS评分,归一化至基线。用MADRS评分计算各组的响应率(response)和缓解率(remission)。响应定义为MADRS评分下降至少50%,缓解定义为MADRS评分下降不大于10。在4周的随访中,如果参与者在任何时候满足了这些特定的症状,他们就被认定为响应者或缓解者。选择这种方法,而不是选择在单一时间点的响应或缓解,可以考虑不同的响应轨迹。这种计算响应率和缓解率的方法是专门选择的,作为重度抑郁症快速治疗疗法开发的一部分,这种快速治疗与全面的长期治疗相结合,以保持参与者处于缓解状态。因此,该方法的缓解率最相关的衡量指标是在治疗后一个月内任何时间点进入缓解期的个体比例,无论他们是在治疗后立即进入缓解期还是在延迟反应轨迹后进入缓解期,因为不管治疗轨迹如何,都会进行维持治疗。6-项HAM-D、17-项HAM-D和QIDS-SR得分的变化被用作抑郁严重程度的次要测量指标。初始线性混合模型产生的残差不是正态分布的(通过Shapiro-Wilk检验评估)。因此,使用广义线性混合模型评估MADRS、6-项HAM-D、17-项HAM-D和QIDS-SR得分的变化,该模型使用Satterthwaite自由度近似和稳健系数估计来处理违反模型假设的情况。评估时间、治疗组(真或假)的固定效应和交互效应。除模型不收敛或收敛于非实解的情况外,所有分析均采用复合对称协方差结构。在这些情况下,使用了自回归协方差结构。所有事后两两比较都经过了Bonferroni校正。类似的广义线性混合模型被用于分析潜在的神经认知副作用。
3结果
3.1被试特征
试验在中点停止,因为计划的中期分析表明,与假刺激相比,真刺激的效应值较大(Cohen’d>0.8)。因此,这里报告的结果来自于进入试验直至中期分析的参与者样本。
共有182人通过在线筛查数据库进行了资格评估,其中54人接受了现场筛查。32名参与者进行了随机分组;然而,其中两名参与者没有被纳入,一名因为不再符合纳入标准而退出,另一名因为厌恶可能被分配到假刺激组而退出。剩下的30名参与者以1:1的比例被分配接受真或假SNT。在纳入后,另一名参与者被发现不符合纳入标准。因此,符合纳入标准、加入试验并同意接受真或假治疗的两组参与者的最终人数分别为真SNT组14人和假SNT组15人(图2)。两组的人口统计学特征相似(表1)。两组的既往抗抑郁药物试验数量(均值=5,SD=2)和Maudsley分期法总得分(均值=9,SD=2;中度抗药性)相同。所有参与者都完成了全面治疗和治疗后即刻评估。两组各有1例患者未完成4周随访。假治疗组的一名参与者在研究入组后,SNT治疗周前2周开始服用一种新的药物(5 -羟色胺-肾上腺素再摄取抑制剂),在整个试验中一直保持亚治疗剂量水平。所有的分析都包括了这个参与者。

图2难治性抑郁症患者真或假斯坦福神经调控治疗(Stanford neuromodulation therapy, SNT)前后的抑郁评分
 表1 斯坦福神经调控治疗(Stanford neuromodulation therapy, SNT)双盲随机对照试验参与者的特征
表1 斯坦福神经调控治疗(Stanford neuromodulation therapy, SNT)双盲随机对照试验参与者的特征3.2效力(Efficacy)
最初的主要结果是5天SNT治疗结束后4周的MADRS评分。评分归一化到治疗前基线,即以基线值的百分比表示。真刺激组治疗后0周、1周、2周、3周和4周的意向治疗(intention-to-treat) MADRS得分的平均降低百分比是基线的62.0%、70.9%、62.4%、57.8%、52.5%,假刺激组是14.3%、20.6%、10.4%、10.9%和11.1%,效应值(Cohen’s d)分别为1.7、1.4、1.8、1.5、1.4。由于参与者的响应轨迹不同,响应率和缓解率随随访时间点而变化。总的来说,在4周的随访中,真SNT组中有12名(85.7%)参与者符合响应标准(MADRS评分降低超过50%),11名(78.6%)参与者在5个治疗后评估中至少有一个达到缓解标准(MADRS评分不大于10)。在假治疗组,4周随访期间,4名参与者(26.7%)有反应,2名参与者(13.3%)在某个时间点缓解。真治疗组治疗后0、1、2、3、4周的缓解率和响应率分别为57.1%和71.4%;66.7%和77.8%;53.8%和84.6%;61.5%和69.2%;46.2%和69.2%。假刺激的缓解率和响应率分别为0%和13.3%;10.0%和20.0%;7.1%和7.1%;7.1%和7.1%;0%和7.1%。
广义线性混合模型显示,在MADRS评分上,治疗组(F=24.8, df=1, 14, p<0.001)、时间(F=16.1, df=5, 24, p<0.001)的主效应显著,治疗组与时间(F=6.1, df=5, 24, p<0.001)的交互效应显著。真治疗组的参与者在所有随访时间点的MADRS评分在治疗后显著降低(Bonferroni校正p<0.05)。对于次要结果(6-项HAM-D、17-项HAM-D和QIDS-SR得分的变化)、使用上次观察结转法(last-observation-carried-forward method)估算的缺失数据模型,以及使用原始评分而不是基线评分时,发现了等价的结果。
3.3盲法的完整性
23名参与者猜测了他们所接受的是哪种治疗,19名参与者表示对自己的猜测有信心。单因素t检验表明,假刺激组(平均猜值=0.39,p=0.56)和真刺激组(平均猜值=0.43,p=0.52)的随机性(随机值=0.50)没有显著差异。因为并不是所有的参与者都对自己的猜测有信心,所以二项测试也被用来确定正确猜测的次数是否超过了随机水平。二项测试表明,在假刺激(6/10正确,p=0.38)和真刺激组(7/13正确,p=0.50)中,正确猜测的比例与随机水平没有显著差异。在MADRS评分中,猜测度量和评分比例变化幅度之间没有关系(r=0.11, p=0.66)。因为使用了两种假刺激方法,我们还测试了两种方法之间的差异,即正确猜测自己属于假治疗组的参与者的比例,我们发现没有显著差异(Fisher的确切测试,p=0.12)。此外,在广义线性混合模型中纳入假刺激类型并没有改变结果,假刺激类型或假刺激类型与时间的相互作用也不是一个显著因素(假刺激类型:F=0.2, df=1,21, p=0.68;治疗组:F=26.6, df=1, 19, p<0.001;时间:F=13.2, df=5, 38, p<0.001;治疗组-时间交互作用:F=5.8, df=5, 33, p=0.001;假刺激类型与时间的交互作用:F=1.9, df=4, 29, p=0.14)。
3.4安全性
试验期间未发生严重不良事件。每天记录自发的副作用,并按常见的rTMS副作用进行分类。如果不适只发生在刺激过程中,而在SNT后没有持续,则记录“治疗部位不适”;如果不适在治疗后持续,则记录“SNT后头痛”。与假刺激组相比,真刺激组的唯一副作用发生率接近统计学意义的是头痛(Fisher确切检验,p<0.06)。所有头痛自行缓解或在服用非处方止痛药(如布洛芬)后缓解。两组患者最常见的副作用是疲劳。在另一项试验中,一名参与者经历了牙齿脱落,之后我们改变了实验室中所有试验的牙齿安全协议,包括目前的试验。
从基线到治疗后即刻评估,真假治疗组均表现出稳定的认知测试表现。语言加工速度(颜色单词阅读完成时间)存在组别和时间的显著交互作用(F=4.7, 1,21, p=0.04),随后的Bonferroni校正的事后比较显示,真刺激组有显著改善(F=5.5, df=1,21, p=0.03),假刺激组没有(F=0.4, df=1,21, p=0.54)。所有其他测量显示,组别和时间的交互作用不显著。
4.讨论
本研究的目的是研究SNT的抗抑郁疗效,SNT是一种加速、高剂量、模式化、fcMRI指导的iTBS方案,用于治疗难治性抑郁症。参与者对治疗的耐受性良好;所有参与者都完成了5天的疗程,副作用与常规每日rTMS相似,真SNT组的头痛发生率高于假治疗组。头痛是TMS治疗方案中最常见的副作用之一,所以这是预期的副作用;我们的真治疗组的头痛发生率(57%)与FDA批准的治疗难治性抑郁症的标准iTBS方案(65%)相似。
我们观察到SNT有很大的抗抑郁作用。经过5天的治疗后,真SNT组79%的参与者(14名参与者中的11名)在4周的随访中在某个时间点抑郁发作得到缓解,而假治疗组只有13% (15名参与者中的2名)。SNT治疗疗程短,抗抑郁疗效高,为需要快速治疗的急诊或住院患者提供了治疗机会。
SNT的大效应可能是由几个因素造成的。SNT方案是根据神经科学信息的刺激参数设计的,并被选择以最佳方式调节目标神经回路。
首先,fcMRI引导的靶向策略用于刺激每个个体中与sgACC最负相关的左侧DLPFC区域。
第二,刺激每小时进行一次,因为50到90分钟的间隔已经被证明对突触强化产生累积效应。相比之下,间隔40分钟或更短的间隔不会产生累积效应。
第三,我们以静息运动阈值(rMT)的90%的强度进行刺激,并根据靶区皮层深度的个体差异进行调整,而不是FDA批准的rMT强度的120%,因为90%的rMT强度下,传递1800次脉冲可能更有效地诱导皮质兴奋性的改变由此产生的功能连通性改变。
第四,每个iTBS治疗发出1800次脉冲,而不是典型的600次脉冲,因为在90%的rMT强度下,1800次iTBS脉冲已被证明在皮质兴奋性方面产生更大的变化。此外,一项使用1800次脉冲的盲法iTBS试验仅在2周内就产生了有效的抗抑郁反应,这比FDA批准的使用600次脉冲的标准iTBS方案要快。最后,SNT方案被设计为提供比标准iTBS方案更高的总脉冲剂量(90000和18000次脉冲),因为更高的脉冲剂量与更大的抗抑郁疗效相关。SNT参数的选择在我们之前的出版物中进行了详细的讨论。
尽管我们的受试者样本中抑郁症状的严重程度和难治性水平很高,并且在1个月的随访中进行了计算,但仍观察到SNT的抗抑郁作用量很大。更严重的抑郁症状和更高水平的难治性都与rTMS反应较差有关。我们研究的参与者平均有五次适当的抗抑郁药物试验;传统的rTMS疗法被发现只有17%的患者有缓解,这些患者之前对三种抗抑郁药物治疗没有反应。此外,62%的参与者有复发性抑郁发作,而不是连续发作,这也被证明对rTMS治疗后的结果有负面预测。与rTMS研究中假治疗通常报告的缓解率相比,在我们的样本中,高水平的治疗耐药性也可能是我们假治疗组的缓解率相对较低的原因(13%);之前的一项假对照iTBS研究表明,中度至重度治疗抵抗的个体对假治疗的反应最小。
在这份报告中,我们包括了整个4周随访期的响应率和缓解率。这与其他iTBS抑郁症临床试验中更常见的单时间点响应或缓解标准不同。我们认为,基于SNT作为抑郁症状潜在神经回路的探针和预期的未来临床方法,这种定义二分类结果的方法是合适的。这些高的总体响应率和缓解率提供了进一步的证据,支持左侧DLPFC-sgACC网络的功能障碍是抑郁症状的主要神经基础。本研究在文献的基础上进行了扩展,证明当使用优化的刺激剂量和模式来定位该回路时,绝大多数个体(本研究中85.7%)将在一段时间内产生抗抑郁反应。由于未知的原因,参与者在SNT过程中显示出不同的反应轨迹(见图2E),这在rTMS和iTBS中已被报道。作为一种治疗工具,SNT仍在开发中。我们提出了一种治疗模式,在这种治疗模式中,SNT被用于快速缓解抑郁症,随后进行强度较小的维持治疗,可以采用任何有效和可接受的方式——药物、心理治疗、脑刺激和其他治疗。在这种治疗模式下,所有在治疗后一个月进入缓解期的患者都可以过渡到维持治疗。因此,通过在4周随访期间任何一周内符合这些标准的所有参与者来计算响应率和缓解率是合适的。
这项研究有一些局限性:
首先,由于真治疗组的优势和较大的效应量,试验在计划的中期分析时结束,因此,样本量小;然而,样本量与其他针对严重难治性抑郁症患者的临床试验的样本量相似。
其次,与所有重度抑郁症的临床试验一样,我们的研究依赖于临床评估来衡量抑郁症症状的改善,因为目前还没有抑郁症缓解的有效生物标志物。
第三,到目前为止,我们的SNT方案已经在一个单一的地点,在一个受过高等教育的样本中进行了测试。虽然这限制了推广,但在这个治疗抵抗人群中没有显著的假反应,表明真刺激对这个患者群体的疗效明显优于假刺激。
第四,45%的参与者样本有精神疾病共病,这可能会影响方案的有效性。尤其是共病焦虑会降低rTMS的效力,也许是因为这些患者需要一个替代的治疗靶点或该人群中苯二氮卓类药物使用率更高。然而,真治疗组和假治疗组共病精神疾病的参与者人数没有显著差异。
最后,考虑到与其他TMS方案相比,在类似人群中效果较大,我们假设SNT和标准rTMS方案之间的差异导致了较高的抗抑郁疗效;然而,SNT仍需直接针对另一种真刺激方案进行测试,SNT方案在改善传统iTBS疗效方面的独特性仍有待确定。需要进行研究,比较有无fcMRI引导靶向的SNT参数的有效性,以确定这种靶向方法的重要性。
总之,在难治性样本中,经过5天的治疗后,与相同的假刺激疗程相比,SNT能显著降低抑郁症状。短时间和高抗抑郁效果的SNT可以在紧急或住院情况下治疗患者,在这种情况下压缩时间过程是必要的。
总结:
本文提出了个性化斯坦福神经调控疗法,作者使用静息态功能MRI定位个体化靶点,即左侧背外侧前额叶皮层与膝下前扣带皮层功能负相关最强的区域。该个体化靶点用于难治性抑郁症患者治疗,比假刺激治疗更有效。该疗法加速、高剂量、模式化、以功能连接为指导确定个体化靶点,疗程短,抗抑郁疗效高,为需要快速治疗的急诊或住院患者提供了治疗机会
————————————————
版权声明:本文为CSDN博主「思影科技」的原创文章,遵循CC 4.0 BY-SA版权协议,转载请附上原文出处链接及本声明。
原文链接:https://blog.csdn.net/cc1609130201/article/details/123705647www.psychspace.com心理学空间网

